| > | restart:#"m09_p12" |
En la producción de gas ciudad a partir de gas natural entran en juego las dos reacciones CH4+H2O=CO+3H2 y CO+H2O=CO2+H2. Considerando que se alcanza el equilibrio, se pide:
a) ¿Qué será más conveniente, producir el gas a 0,1 MPa o a 10 MPa?
b) ¿Qué sería mejor, que el reactor alcanzase una temperatura de 600 K o de 1300 K?
c) Estimar la relación molar entre el H2 y el CO en el punto óptimo de los dos apartados anteriores, suponiendo alimentación equimolar de H2O y CH4.
d) Repetir el apartado anterior pero con alimentación de vapor y metano en relación molar 2:1.
e) Determinar la razón de mezcla de la alimentación para que en el caso del apartado c) la concentración de hidrógeno producida sea máxima.
f) Calcular el flujo de calor en el caso del apartado d), suponiendo que la mezcla entra a 600 K.
g) ¿Es posible que a la salida se deposite carbono por la reacción 2CO=C+CO2 en el caso c) o en el d)?
Datos:
| > | read`../therm_chem.m`:with(therm_chem):with(therm_proc): |
| > | su1:="Aire":dat:=[p1=1e4*Pa_,T1=1300*K_,b_a1=1,b_a2=2]; |
Esquema:
| > |
Eqs. const.:
| > | dat:=op(dat),op(subs(g=g0,[Const])),SI2,SI1: |
a) ¿Qué será más conveniente, producir el gas a 0,1 MPa o a 10 MPa?
Para la reacción 2ª es indiferente, pero para que la 1ª avance más conviene presiones bajas, luego p = 0,1 MPa es mejor.
| > | eq1:=CH4+H2O=CO+3*H2;eq2:=CO+H2O=CO2+H2;eq3:=2*CO=C+CO2;eq3_:=eqEQ(subs(dat,eq1));i:='i':nu_:=nulist(eq1):C_:=nops(Comp):eq4_:=Sum('nu||i',i=1..C)=sum(nu_[i],i=1..C_);eq5_:=eqEQ(subs(dat,eq2));nu_:=nulist(eq2):eq6:=Sum('nu||i',i=1..C)=sum('nu_[i]',i=1..C_); |
b) ¿Qué sería mejor, que el reactor alcanzase una temperatura de 600 K o de 1300 K?
La 1ª produce más para T > 960 K (done lnK = 0) mientras que la 2ª produce más para T < 970 K, pero cuenta más la 1ª, luego T = 1300 K es mejor
| > | eq3:=eqEQ(subs(dat,eq1));eq7:=hr_=hgs_r25(eq1)[1]:evalf(%,2);Tchange:=solve(subs(p=p0,1=rhs(eq3)),T):'Tchange'=evalf(%,2);eq5:=eqEQ(subs(dat,eq2));eq8:=hr_=hgs_r25(eq2)[1]:evalf(%,2);Tchange:=solve(subs(p=p0,1=rhs(eq5)),T):'Tchange'=evalf(%,2); |
c) Estimar la relación molar entre el H2 y el CO en el punto óptimo de los dos apartados anteriores, suponiendo alimentación equimolar de H2O y CH4.
| > | eqMIX(a*CH4+b*H2O=[4,5,7,8,10]):eq3__:=evalf(subs(p=p1,T=T1,dat,eq3_));eq5_:=evalf(subs(p=p1,T=T1,dat,eq5));sol1:=solve(subs(p=p1,T=T1,b=a*b_a1,dat,dat,{eqNX,eqBC,eqBH,eqBO,eqBN,eq5_,eq3__}),{a,x[Comp[4]],x[Comp[5]],x[Comp[7]],x[Comp[8]],x[Comp[10]]})[4]:'sol1'=evalf(%,2); |
d) Repetir el apartado anterior pero con alimentación de vapor y metano en relación molar 2:1
| > | sol1:=solve(subs(p=p1,T=T1,b=a*b_a2,dat,dat,{eqNX,eqBC,eqBH,eqBO,eqBN,eq5_,eq3__}),{a,x[Comp[4]],x[Comp[5]],x[Comp[7]],x[Comp[8]],x[Comp[10]]})[1]:'sol1'=evalf(%,2); |
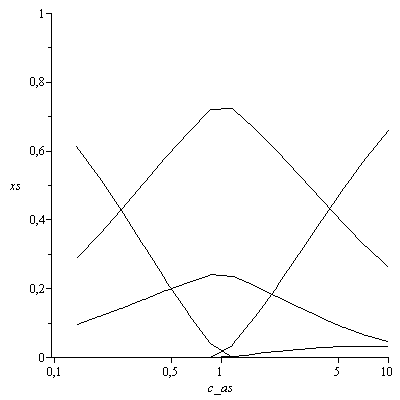
e) Determinar la razón de mezcla de la alimentación para que en el caso del apartado c) la concentración de hidrógeno producida sea máxima.
| > | n:=15:arr:=array(1..n,1..6):for i from 1 to n do b_a:=evalf(10^(-1+2*i/n));sol1:=solve(subs(p=p1,T=T1,b=a*b_a,dat,dat,{eqNX,eqBC,eqBH,eqBO,eqBN,eq5_,eq3__}),{a,x[Comp[4]],x[Comp[5]],x[Comp[7]],x[Comp[8]],x[Comp[10]]})[1]:print(evalf(subs(sol1,[b_a,x[Comp[4]],x[Comp[5]],x[Comp[7]],x[Comp[8]],x[Comp[10]]]),2));arr[i,1]:=b_a;arr[i,2]:=subs(sol1,x[Comp[8]]);arr[i,3]:=subs(sol1,x[Comp[4]]);arr[i,4]:=subs(sol1,x[Comp[5]]);arr[i,5]:=subs(sol1,x[Comp[7]]);arr[i,6]:=subs(sol1,x[Comp[10]])od:pl2:=pla(arr,2,1):pl3:=pla(arr,3,1):pl4:=pla(arr,4,1):pl5:=pla(arr,5,1):pl6:=pla(arr,6,1):with(plots):semilogplot([pl2,pl3,pl4,pl5,pl6],c_as=0.1..10,xs=0..1,color=black); |
 |
f) Calcular el flujo de calor en el caso del apartado d), suponiendo que la mezcla entra a 600 K.
| > | i:='i':Dh:=Dhterm+Dhquim;Dhterm:=(T1-T25)*(x[Comp[4]]*c[p,CO2]+x[Comp[5]]*c[p,H2O]+x[Comp[7]]*c[p,di]+x[Comp[8]]*c[p,di]+x[Comp[10]]*c[p,CO2])/a;Dhterm_:=subs(sol1,c[p,di]=c[p,N2],cpComp,dat,Dhterm):'Dhterm'=evalf(%,2);Dhquim_:=subs(sol1,(x[Comp[4]]*h4_+x[Comp[5]]*h5_+x[Comp[7]]*h7_+x[Comp[8]]*h8_+x[Comp[10]]*h10_)/a):'Dhquim'=evalf(%,2);q_:=Dhterm_+Dhquim_:'q'=evalf(%,2); |
q<0, es decir, exotérmica.
g) ¿Es posible que a la salida se deposite carbono por la reacción 2CO=C+CO2 en el caso c) o en el d)?
| > | eq7:=evalf(subs(p=p1,T=T1,dat,eqEQ(C+CO2=2*CO))):'eq7'=evalf(%,2); |
Podría formarse C a alta p, baja T y b/a bajos.
| > |