| > | restart:#"m17_p03" |
Se trata del aprovechamiento de un manantial geotérmico (agua caliente subterránea) de 20 m3/h de agua a presión y a 130 °C, para generar electricidad utilizando el agua como foco térmico en una máquina de Rankine cuyo fluido de trabajo es n-butano, y que opera entre 0,3 MPa y 1,8 MPa, entrando a la turbina vapor saturado. Se pide:
a) Potencia elĂ©ctrica máxima producible (lĂmite termodinámico).
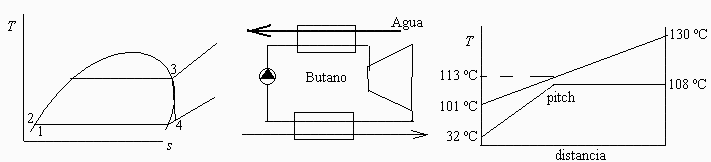
b) Esquema de la instalaciĂłn propuesta y diagrama T s del proceso.
c) Temperaturas extremas del fluido de trabajo.
d) Trabajo especĂfico de la turbina.
e) Gasto másico necesario de butano
f) Potencia generada.
Datos:
| > | read`../therm_eq.m`:read`../therm_const.m`:read`../therm_proc.m`:with(therm_proc): |
| > | su1:="H2O":su2:="C4H10":dat:=[V=(20/3600)*m_^3/s_,Tw=(130+273)*K_,p1=0.3e6*Pa_,p3=1.8e6*Pa_,eta[T]=1]; |
| > |
| > | eqBE:=eq5_43;Wdat:=get_liq_data(su1):gdat:=get_gas_data(su2):ldat:=get_liq_data(su2):get_pv_data(su2):p[v,nbut](T)=pv(T);dat:=op(dat),gdat,ldat,Const,SI2,SI1: |
a) Potencia elĂ©ctrica máxima producible (lĂmite termodinámico).
Será la exergĂa de la corriente de agua respecto al ambiente. SĂłlo se considera la exergĂa termomecánica, psi=h-T0·s, despreciando la exergĂa obtenible del agua en condiciones ambiente respecto a la atmĂłsfera de referencia (dependerĂa de la humedad ambiente, y no serĂa difĂcil obtener algo de esa exergĂa por enfriamiento evaporativo).
Como datos de las sustancias podrĂan usarse diagramas (p-h, h-s...), tabulaciones..., pero vamos a usar el modelo de sustancia perfecta, comparando con los valores más exactos del NIST (DATA).
| > | Wmax:=m*(Dh-T0*Ds);m:=rho*V;rho=subs(Wdat,rho);mw_:=subs(Wdat,dat,rho*V);rho[DATA]:=937.2*kg_/m_^3;m[DATA]:=evalf(subs(dat,rho[DATA]*V),3);Dh:=c*(Tw-T0);Dh_:=subs(Wdat,dat,Dh):'Dh'=evalf(%,2);Ds:=c*ln(Tw/T0);Ds_:=evalf(subs(Wdat,dat,Ds)):'Ds'=evalf(%,2);Wmax_:=subs(dat,evalf(subs(dat,mw_*(Dh_-T0*Ds_)))):'Wmax'=evalf(%,2);WmaxDATA_:=subs(SI0,evalf(m[DATA]*((546000-63000)-288*(1635-225))))*W_:'WmaxDATA'=evalf(%,2); |
i.e. el máximo obtenible es 0,42 MW (con los datos del NIST 0,40 MW).
b) Esquema de la instalaciĂłn propuesta y diagrama T s del proceso.
(Hecho arriba)
c) Temperaturas extremas del fluido de trabajo.
Serán las de cambio de fase a las presiones dadas, pues no hay sobrecalentamiento.
| > | Tvp1_:=fsolve(subs(dat,SI0,pv(T)=p1),T=300..700)*K_;Tvp3_:=fsolve(subs(dat,SI0,pv(T)=p3),T=300..700)*K_;Tvp1=TKC(Tvp1_);Tvp3=TKC(Tvp3_); |
i.e. el n-butano se vaporizará a 108 ºC y condensará a 32 ºC (con datos del NIST, a 108,7 ºC y 32,4 ºC).
d) Trabajo especĂfico de la turbina.
Como la entrada a la turbina es vapor saturado, se podrĂa suponer salida bifásica (como ocurrirĂa en un ciclo de vapor de agua), pero las molĂ©culas grandes presentan retroceso en la lĂnea de vapor saturado:
| > | wet_vap(Tvp3_,subs(dat,p3),subs(dat,p1)); |
luego sale todo vapor (y no mezcla bifásica). En función del rendimiento isoentrópico de la turbina:
| > | eq5_60;T4_:=solve(eq5_60,T4);eta=subs(dat,eta[T]);'gamma'=subs(dat,gamma);T4_:=subs(T3=Tvp3_,eta=eta[T],pi[12]=p3/p1,dat,T4_);'T4'=TKC(T4_);h1_:=subs(dat,T=Tvp1_,dat,hl(T));h2=h1;h3_:=subs(dat,T=Tvp3_,dat,hv(T));h4_:=subs(dat,T=T4_,dat,hv(T));q23=h3-h2;q23_:=h3_-h1_;w34=h3-h4;w34_:=h3_-h4_;eta[e]=w34/q23;eta[e]=evalf(w34_/q23_); |
![eta = `/`(`*`(`+`(1, `-`(`/`(`*`(T4), `*`(T3))))), `*`(`+`(1, `-`(`^`(`/`(1, `*`(pi[12])), `/`(`*`(`+`(gamma, `-`(1))), `*`(gamma)))))))](images/p03_24.gif) |
![`+`(`*`(eta, `*`(T3, `*`(`^`(`/`(1, `*`(pi[12])), `/`(`*`(`+`(gamma, `-`(1))), `*`(gamma)))))), `-`(`*`(eta, `*`(T3))), T3)](images/p03_25.gif) |
Con datos del NIST:
| > | h1data:=276.5e3;h3data:=730.5e3;h4data:=656.2e3;q23data:=h3data-h1data;w34data:=h3data-h4data;eta=evalf(w34data/q23data); |
La discrepancia es apreciable (del orden del 20%) y en contra.
NĂłtese que el valor de las entalpĂas depende mucho del estado de referencia elegido: en el modelo de sustancia perfecta hemos tomado h=0 para el lĂquido en el punto triple, mientras que los datos del NIST estaban referidos al estándar IIR (International Institute of Refrigeration, que toma h=200 kJ/kg para el lĂquido saturado a 0 ÂşC).
e) Gasto másico necesario de butano.
Hay que calentar el butano desde Tvp1 a Tvp2 y vaporizarlo a Tvp2, todo ello con una corriente finita de agua que entra a Tw y no se sabe a quĂ© T sale. Dejando un salto mĂnimo DT=5 ÂşC (extremo o 'pitch', ver dibujo), serĂa Tpitch=Tvp3+DT y en aproximaciĂłn lineal Tsale=Tw-(Tw-Tpitch)*(h3-h1)/(h3-hpitch).
| > | eqBECC:=mb*(h3-h2)=mw*c*(Tw-Tsale);DT_:=5*K_;Tpitch=Tvp3+DT;Tpitch_:=Tvp3_+DT_;Tpitch=TKC(Tpitch_);Tsale=Tw-(Tw-Tpitch)*(h3-h1)/(h3-hpitch);hpitch_:=subs(dat,T=Tpitch_,dat,hl(T)):hpitch=evalf(%,2);Tsale_:=subs(dat,Tw-(Tw-Tpitch_)*(h3_-h1_)/(h3_-hpitch_));Tsale=TKC(Tsale_);Q23:=mw*cw*(Tw-Tsale);Q23_:=subs(Wdat,dat,mw_*c*(Tw-Tsale_));mb_:=subs(Wdat,dat,mw_*c*(Tw-Tsale_)/(h3_-h1_));mbDATA_:=subs(Wdat,dat,SI0,m[DATA]*c*(Tw-Tsale_)/(h3data-h1data))*kg_/s_; |
i.e. el agua no puede salir más frĂa de 101 ÂşC, transmitiendo Q=670 kW de calor al ciclo, por el que ha de circular 1,5 kg/s de n-butano (1.4 kg/s con datos NIST).
f) Potencia generada
| > | W34:=mb*(h3-h4);W34_:=subs(dat,mb_*(h3_-h4_));WDATA_:=evalf(subs(dat,mbDATA_*w34data));eta='W34/Q23';eta=W34_/Q23_; |
i.e. con este ciclo se generarĂan 0,13 MW de trabajo en vez del lĂmite termodinámico de 0,42 MW (con datos NIST, 0,10 MW y 0,40 MW, respectivamente).
Como comprobación hemos vuelto a calcular el rendimiento energético del ciclo.
NĂłtese la mejora que supone en todos estos ciclos ORC (Organic Rankine Cycle) la introducciĂłn de un regenerador que aproveche la entalpĂa del vapor de 4 a 4v, para calentar un poco el lĂquido de 1 a 1' (ver Fig. 2).
| > |
