| > | restart:#"m15_p58" |
| > | read`../therm_eq.m`:read`../therm_chem.m`:with(therm_chem);with(therm_proc): |
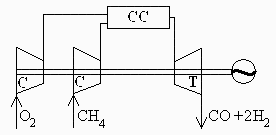
Se quiere producir un flujo de 0,1 kg/s de hidrógeno a partir de gas natural (supóngase metano). En lugar de hacerlo mediante reformado con vapor como es habitual, se quiere estudiar la posibilidad de hacerlo mediante oxidación parcial con oxígeno puro en una cámara de combustión a 1 MPa, según la reacción CH4+(1/2)O2=CO+2H2, pretendiéndose además generar electricidad por expansión de los gases producto en una turbina que movería un alternador y los compresores de gas natural y de oxígeno. Se pide:
a) Poder calorífico de dicha reacción, y gastos de gases reactivos.
b) Temperatura de entrada a la cámara de los gases reactivos, y temperatura de salida de los gases producto.
c) Electricidad que se generaría.
Datos:
| > | su1:="CH4":su2:="O2":su3:="CO":su4:="H2":dat:=[mH2=0.1*kg_/s_,p2=1e6*Pa_];eq:=CH4+(1/2)*O2=CO+2*H2; |
Eqs. const.:
| > | dat:=op(subs(g=g0,[Const])),op(dat),SI2,SI1:CH4dat:=get_gas_data(su1):O2dat:=get_gas_data(su2):COdat:=get_gas_data(su3):H2dat:=get_gas_data(su4): |
a) Poder calorífico de dicha reacción, y gastos de gases reactivos.
| > | eq15_5;PC_:=PCI(eq);nH2=mH2/MH2;nH2_:=subs(H2dat,dat,mH2/M);eq;nCO='nH2/2';nCO_:=nH2_/2;nCH4_:=nH2_/2;nO2_:=nH2_/4;mCH4_:=subs(CH4dat,dat,nCH4_*M);mO2_:=subs(O2dat,dat,nO2_*M);mCO_:=subs(COdat,dat,nCO_*M); |
i.e., el poder calorífico es de 35,7 kJ/mol (de metano), y se necesitan 0,4 kg/s de metano y 0,4 kg/s de oxígeno (generándose 0,7 kg/s de CO más los 0,1 kg/s de H2).
Nótese que la relación combustible/comburente, 67% de metano en la mezcla, está por encima del límite superior de ignición, por lo habrá que producir el encendido durante la mezcla y no una vez mezclado.
b) Temperatura de entrada a la cámara de los gases reactivos, y temperatura de salida de los gases producto.
Como no nos dan más datos, supondremos compresores ideales (se mejoraría el modelo poniendo un valor típico).
| > | eqComp:=T2=T0*(p2/p0)^((gamma-1)/gamma);gamma[CH4]=subs(CH4dat,gamma);eqCH4:=subs(CH4dat,dat,eqComp);gamma[O2]=subs(O2dat,gamma);eqO2:=subs(O2dat,dat,eqComp);eqBE_CC:=(mCO*c[p,CO]+mH2*c[p,H2])*(Tad-T25)=mCH4*c[p,CH4]*(T2_CH4-T25)+mO2*c[p,O2]*(T2_O2-T25)+nCH4*PC;Tad_:=solve(eqBE_CC,Tad);Tad__:=subs(nCH4=nCH4_,PC=PC_,mCH4=mCH4_,mO2=mO2_,mCO=mCO_,c[p,CH4]=c[p],CH4dat,c[p,O2]=c[p],O2dat,c[p,CO]=c[p],COdat,c[p,H2]=c[p],H2dat,T2_CH4=T2,eqCH4,T2_O2=T2,eqO2,dat,Tad_); |
i.e., la temperatura de salida de la cámara de combustión es de unos 830 K, aunque se han usado los valores de c[p] a temperatura ambiente (al aumentar c[p] con la temperatura, la Tad sería algo menor, pero la T2 de entrada tambiénsería mayor con compresores no ideales, así que se compensarán algo.
c) Electricidad que se generaría.
Supondremos también turbina ideal porque no nos dan el rendimiento (se mejoraría el modelo poniendo un valor típico).
| > | Wt:=m*c[p]*(T3-T4);Wt:=(mCO*c[p,CO]+mH2*c[p,H2])*Tad*(1-(p0/p2)^((gamma-1)/gamma));gamma[CO]=subs(COdat,gamma);gamma[H2]=subs(H2dat,gamma);eqg:=gamma=1.4;Wt_:=subs(eqg,mCO=mCO_,c[p,CO]=c[p],COdat,c[p,H2]=c[p],H2dat,Tad=Tad__,dat,Wt);Wc_CH4:=mCH4*c[p,CH4]*(T2_CH4-T0);Wc_CH4_:=subs(CH4dat,eqCH4,dat,mCH4_*c[p]*(T2-T0));Wc_O2_:=subs(O2dat,eqO2,dat,mO2_*c[p]*(T2-T0));Wnet:='Wt-Wc_CH4-Wc_O2';Wnet_:=Wt_-Wc_CH4_-Wc_O2_; |
i.e. se podría generar algo menos de 0,6 MW de electricidad, además del hidrógeno deseado (que habría que separar del CO después).
| > |