| > | restart;#"m07_p33" |
Se mezcla 1 litro de metanol con 1 litro de etanol a presión ambiente. Suponiendo que la mezcla es ideal, se pide:
a) Fracciones másicas y molares en la mezcla.
b) Temperatura de ebullición de la mezcla.
c) Composición de la mezcla a 70 ºC y 100 kPa.
d) Volumen de la mezcla (masa total) en esas condiciones.
Datos:
| > | read"../therm_eq.m":read"../therm_proc.m":with(therm_proc): |
| > | su1:="CH4O":su2:="C2H6O":dat:=[V01=1e-3*m_^3,V02=1e-3*m_^3,Tm=(70+273)*K_]; |
Esquema:
| > |
Eqs. const.:
| > | dat:=op(dat),Const,SI2,SI1:dat1:=get_gas_data(su1),get_liq_data(su1):dat2:=get_gas_data(su2),get_liq_data(su2):pv1:=proc(T) global su1;get_pv_data(su1);RETURN(pv(T)):end: pv2:=proc(T) global su1;get_pv_data(su2);RETURN(pv(T)):end:rho1_:=subs(dat1,rho);rho2_:=subs(dat2,rho);pv1=pv1(T),pv2=pv2(T);Tb1_:=subs(dat1,T[b]);'Tb1_'=TKC(%);Tb2_:=subs(dat2,T[b]);'Tb2_'=TKC(%); |
a) Fracciones másicas y molares en la mezcla.
| > | eqBMas:=mt=m1+m2;m1:=V1*rho1;m1_:=subs(dat,V01*rho1_);n1:='m1/M1';n1_:=subs(dat1,m1_/M);m2_:=subs(dat,V02*rho2_);n2_:=subs(dat2,m2_/M);y1:=m1/(m1+m2);eqBMol:=nt=n1_+n2_;y1_:=m1_/(m1_+m2_);eqx0:=x1='n1/(n1+n2)';x1_:=n1_/(n1_+n2_); |
i.e., hay prácticamente un 50% en peso de metanol, o, lo que es lo mismo, un 59% en base molar de metanol (y el resto hasta el 100% etanol).
b) Temperatura de ebullición de la mezcla.
Habrá de ser del orden de la semisuma de las de los compuestos puros. Se calcula con la ecuación de Raoult, sabiendo que al empezar la ebullición la concentración del líquido es la dada.
Por consistencia, volvemos a determinar los valores de ebullición con la ecuación de Antoine.
| > | Tb1_:=evalf(subs(dat,dat1,solve(p0=pv1(T),T)));'Tb1_'=TKC(%);Tb2_:=evalf(subs(dat,dat2,solve(p0=pv2(T),T)));'Tb2_'=TKC(%);eqE1:=xv1/xl1=pv1/p;eqE1_:=subs(xl1=x1_,pv1=pv1(Tb),p=p0,dat,%);eqE2:=xv2/xl2=pv2/p;eqE2_:=subs(dat,subs(xv2=1-xv1,xl2=1-x1_,pv2=pv2(Tb),p=p0,dat,%));solb_:=solve({eqE1_,eqE2_},{Tb,xv1});'Tb'=TKC(subs(solb_,Tb)); |
La mezcla empezaría a hervir a 69,2 ºC. Para saber cuando acabaría de hervir habría que determinar la temperatura de condensación.
| > | eqE1_:=subs(xv1=x1_,pv1=pv1(Tc),p=p0,dat,eqE1);eqE2_:=subs(dat,subs(xv2=1-x1_,xl2=1-xl1,pv2=pv2(Tc),p=p0,dat,eqE2));solc_:=fsolve(subs(SI0,{eqE1_,eqE2_}),{Tc,xl1},Tc=300..400);Tc_:=subs(solc_,Tc*K_);'Tc'=TKC(%); |
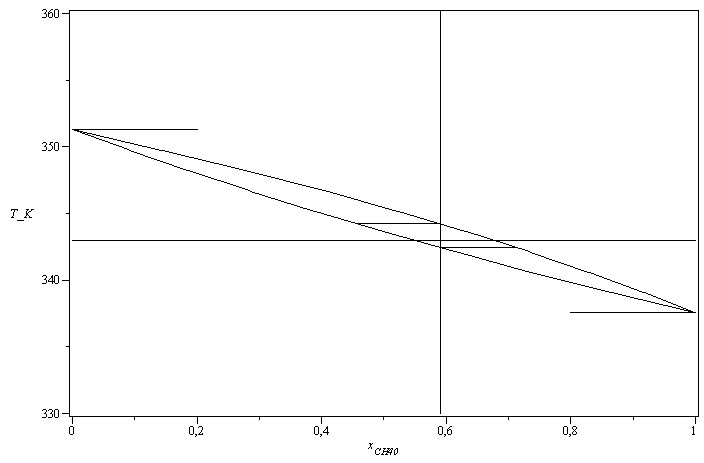
i.e., empieza a hervir a 69,2 ºC y acaba con todo el líquido a 71,0 ºC. Ya de paso se puede dibujar todo el diagrama T-x de las mezclas metanol/etanol.
| > | eqNV:=xv1+xv2=1;eqNL:=xl1+xl2=1;eqC1:=xv1*xv0+xl1*xl0=x01;eqC2:=xv2*xv0+xl2*xl0=x02;eqE1:=xv1/xl1=pv1/p;eqE2:=xv2/xl2=pv2/p;sol1:=solve({eqNV,eqNL,eqE1,eqE2},{xv1,xv2,xl1,xl2});sol2:=solve({eqC1,eqC2},{xv0,xl0});n:=9:for i from 0 to n do T||i:=Tb1_+(Tb2_-Tb1_)*(i/n);xv1||i:=subs(sol1,p=p0,dat,pv1=pv1(T||i),pv2=pv2(T||i),dat1,SI0,xv1);xl1||i:=subs(sol1,p=p0,dat,pv1=pv1(T||i),pv2=pv2(T||i),dat1,SI0,xl1);od:plot({[seq([xv1||i,T||i/K_],i=0..n)],[seq([xl1||i,T||i/K_],i=0..n)],[[0,Tb2_/K_],[.2,Tb2_/K_]],[[1,Tb1_/K_],[.8,Tb1_/K_]],[[x1_,0],[x1_,1000]],[[0,subs(dat,Tm/K_)],[1,subs(dat,Tm/K_)]],[[subs(solc_,xl1),Tc_/K_],[x1_,Tc_/K_]],[[subs(solb_,xv1),subs(solb_,Tb)/K_],[x1_,subs(solb_,Tb)/K_]]},x[CH40]=0..1,'T_K'=330..360,color=black,axes=boxed); |
 |
c) Composición de la mezcla a 70 ºC y 100 kPa.
| > | pv1_:=subs(dat,evalf(subs(dat,pv1(Tm))));pv2_:=subs(dat,evalf(subs(dat,pv2(Tm))));sol_:=subs(dat,evalf(subs(p=p0,pv1=pv1(Tm),pv2=pv2(Tm),dat,sol1))); |
Puede verse la correspondencia con el gráfico.
d) Volumen de la mezcla (masa total) en esas condiciones.
Será aproximadamente el de la fase gaseosa.
| > | V:=nv*R[u]*Tm/p0;sol2_:=subs(x01=x1_,x02=1-x1_,sol_,sol2);nv:=xv0*nt;nv_:=subs(sol2_,xv0*(n1_+n2_));V_:=subs(dat,nv_*R[u]*Tm/p0); |
i.e. la mezcla, si no se deja escapar masa, ocupará 400 litros. Nótese que el litro adicional de líquido restante es irrelevante en volumen.
| > |